Governo de SP havia prometido apresentar nesta quarta-feira ao público e à Anvisa resultados da conclusão dos estudos clínicos
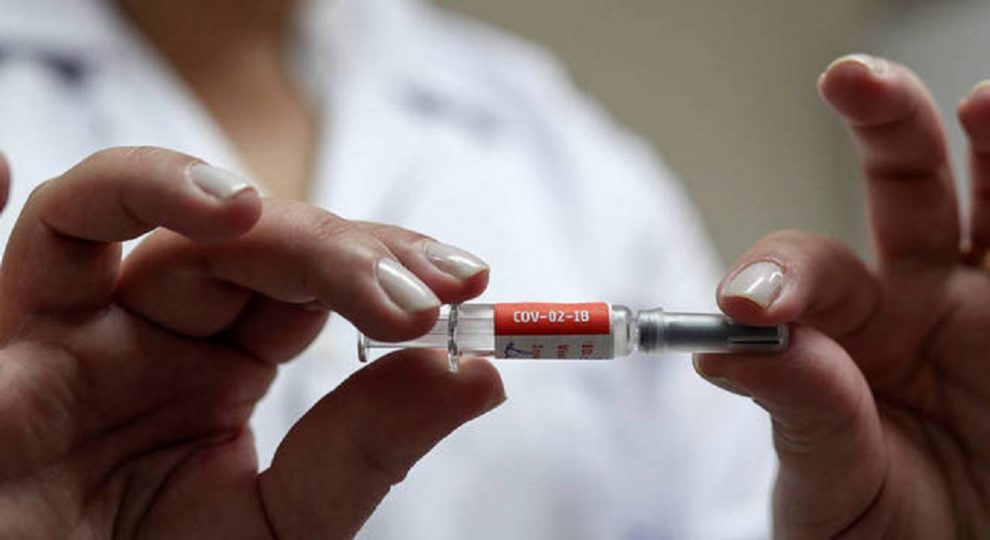
Vai ficar para 2021 o pedido de registro da vacina contra a covid-19 CoronaVac junto à Anvisa (Agência Nacional de Vigilância Sanitária). O governo de São Paulo, que tinha prometido apresentar os resultados dos testes nesta quarta-feira (23), precisou adiar a entrega dos documentos, confirmaram fontes à Record TV.
Esta é a segunda vez que o pedido de registro é postergado — inicialmente, seria em 15 de dezembro.
O argumento é de que a Sinovac, parceira chinesa do Instituto Butantan no desenvolvimento do imunizante contra a covid-19, pediu mais tempo para consolidar dados de testes em países além do Brasil (Turquia e Indonésia).
Devido à restrição imposta pela Sinovac, O Butantan não divulgou o percentual de eficácia da CoronaVac nesta quarta-feira.
O diretor do instituto, Dimas Covas, resumiu apenas que a vacina tem “o limiar da eficácia que permite o processo de solicitação do uso emergência, seja aqui no Brasil ou seja na China”, que é de no mínimo 50% de proteção.
“A Sinovac tem vários estudos clínicos em andamento, ela tem dados nossos e de outros locais. É importante que ela faça uma uniformização de dados, ela não pode analisar dados da mesma vacina com critérios diferentes. Então, este é o motivo principal, da mesma forma como ela não pode ter três eficácias para a mesma vacina”, explicou Dimas Covas.
O anúncio do adiamento do registro da CoronaVac ocorre no dia anterior à chegada de mais de 5 milhões de doses do imunizante a São Paulo, importadas da fábrica da Sinovac em Pequim.
No Brasil, a CoronaVac será submetida a dois processos: registro sanitário — via normal para autorização de um medicamento, que permite aplicação de forma mais abrangente; e e autorização de uso emergencial — modalidade que permite liberação da vacina para grupos selecionados somente durante a pandemia.
Esta última tem o prazo de dez dias para ter uma resposta da Anvisa. Já o registro sanitário é mais demorado.
Os testes no Brasil foram realizados com cerca de 11 mil voluntários da área da saúde em São Paulo, Distrito Federal, Rio de Janeiro, Minas Gerais, Paraná e Rio Grande do Sul.
Na segunda-feira (21), a Anvisa antecipou a publicação do certificado de Boas Práticas de Fabricação da Sinovac, dias após à inspeção da planta da empresa na China. Este é um dos pré-requisitos para a liberação de uma vacina.
O Butantan prevê ter um total de 10,8 milhões de doses da vacina em solo brasileiro até o fim deste ano.
Apesar do revés, o governo de São Paulo reforçou que está mantido o início da vacinação contra a covid-19 no estado em 25 de janeiro.
Segundo o cronograma, 18 milhões de doses serão aplicadas entre 25 de janeiro e 28 de março. Cada paciente tem que esperar 21 dias entre a primeira dose a segunda.
Veja a divisão de datas por grupo prioritário:
Dose 1
25/01 Profissionais da Saúde, indígenas e quilombolas
08/02 Pessoas com 75 anos ou mais
15/02 Pessoas com 70 a 74 anos
22/02 Pessoas com 65 a 69 anos
01/03 Pessoas com 60 a 64 anos
Dose 2
15/02 – Profissionais da Saúde, indígenas e quilombolas
01/03 – Pessoas com 75 anos ou mais
08/03 – Pessoas com 70 a 74 anos
15/03 – Pessoas com 65 a 69 anos
22/03 – Pessoas com 60 a 64 anos
FONTE: R7.COM RECORD TV
























Add Comment